Top-down纳米蛋白组学研究进展:开拓数字微流控和磁珠样品前处理方法
尽管该技术在少数甚至单个哺乳动物细胞的无标记蛋白质组学应用中已经取得了一定的成果,但这些进展大多分布在于自下而上蛋白质组学(Bottom-up proteomics)。对于自上而下蛋白质组学(Top-down proteomics,TDP)来说,依然具有挑战性。与TDP分析明显较低的灵敏度相关,也因此传统的方法依然需要较大的蛋白质上样量和特殊的样品制备流程。
基于磁珠进行完整Proteoform洗脱的One-pot样品制备方法,该流程在数字微流控设备中进行,随后作者采用该方法完成了对单个秀丽隐杆线虫(C. elegans Nematodes)的Top-down纳米蛋白质组学分析,并对在不同条件下生长的秀丽隐杆线虫进行无标记定量分析,确定了BUP分析无法区分的Proteoform的丰度变化。SP3(Single-pot, solid-phase-enhanced sample preparation)是适用于多种样品类型的One-pot样品制备方法,已经与数字微流控技术(Digital microfluidics, DMF)结合应用于BUP分析,本文中,作者在进行Top-down纳米蛋白质组学样品制备时,依然采取了SP3结合DMF的方案。完整蛋白质与SP3磁珠的结合很稳定,需要洗涤剂混合物洗脱才能够有效地回收蛋白质。为了建立一种高灵敏度的TD纳米蛋白质组学样品制备方法,作者使用了与Nano LC-MS兼容的试剂对SP3完整蛋白进行了洗脱。洗脱的阴性对照为水,通过筛选确定洗脱剂为40 % 甲酸(图1)。为避免蛋白质发生甲酰化,在- 20 °C下进行洗脱。在确定了SP3蛋白质洗脱的有效方法后,作者开始将该方法转化为Top-down纳米蛋白质组学样品分析。为了更好的提高灵敏度,作者采用了先前为传统TD蛋白质组学开发的高场不对称波形离子迁移谱(high-field asymmetric-waveform ion mobility spectrometry, FAIMS)和内部补偿电压(Compensation voltage, CV)(图1C)。
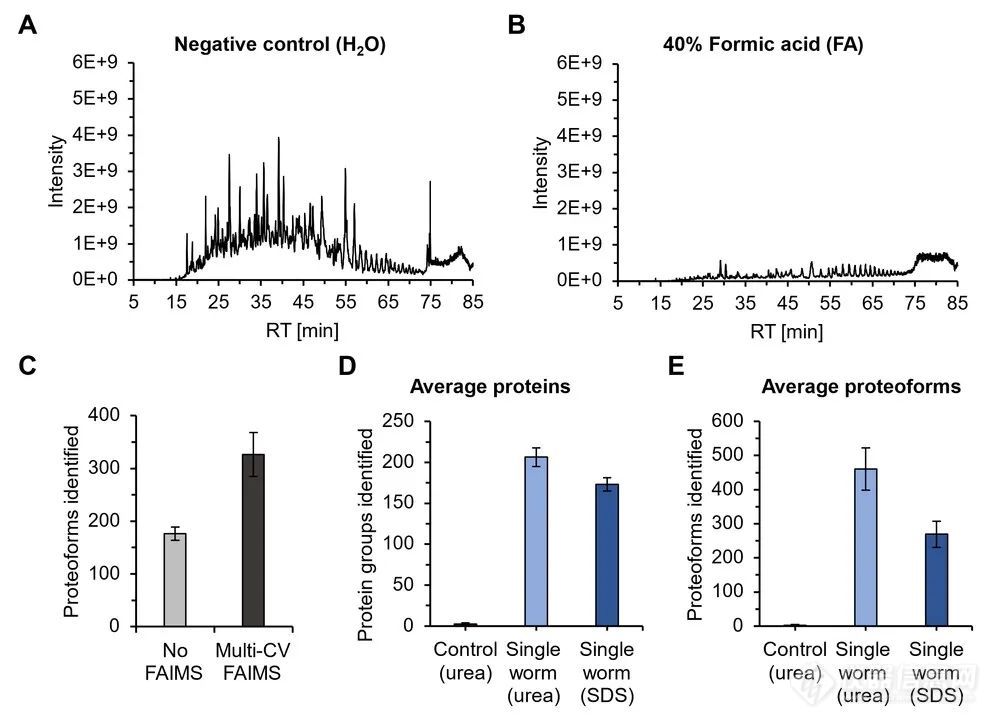
传统的秀丽隐杆线虫蛋白质组学研究一般会用数千个样本来进行,掩盖了单个个体的生物学状态。例如,个别标本已被证明对环境刺激的反应不同。因此,通过在Proteoform水平上对单个个体进行表征,并结合形态、行为和表观遗传学的研究,可以研究群体内的异质性。为了测试基于FA的TD-SP3完整蛋白洗脱的适用性,作者用含有尿素/NP-40表面活性剂或SDS洗涤剂的裂解混合物在PCR管中破坏单个成虫,其中包含恒定数量的959个体细胞,接着进行SP3处理(图1D和E)。处理体积的减少通常被认为是纳米蛋白质组学的灵敏度决定因素。为了进一步微型化TD-SP3,作者在DMF液体控制装置上测试了该方法(图2)。这种技术能够在一系列绝缘和疏水涂层电极上对溶剂液滴进行数字控制操作。通过对选定电极施加电压产生驱动电润湿力,纳米至微升大小的液滴能移动,分裂,或合并。当SP3蛋白被FA有效洗脱时,DMF需要加入钝化洗涤剂来保持含蛋白液滴的流动性。在这里,作者监测了八种不同洗涤剂在C4-RP nano-LC柱上的保留情况。相比之下,一种新型甘露醇基两亲化合物MNA-C12(perGlu-bisdodecyl mannitol),仅在具有高有机溶剂含量的梯度中被洗脱(图 3A)。由于这种非离子型洗涤剂导致DMF上的液滴具有合理的迁移,因此在基于微型化TD纳米蛋白质组学策略中,对DMF-SP3样品做处理时,先用40% FA洗脱蛋白,随后用MNA-C12水溶液稀释。通过对TD-DMF-SP3制备的单个虫做多元化的分析,鉴定出673 ± 69(n=3)种Proteoform,平均对应313 ± 18个蛋白组(图3B)。有必要注意一下的是,与试管内尿素处理(461 ± 62)相比,芯片上TD-SP3导致Proteoform鉴定增加46 %(图3C)。随后作者对热诱导的蛋白质组变化进行了无标记定量分析(图3 D)。
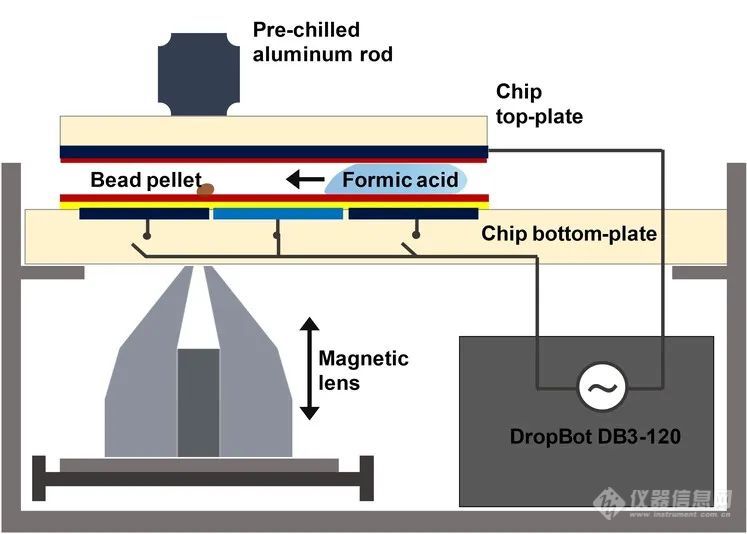
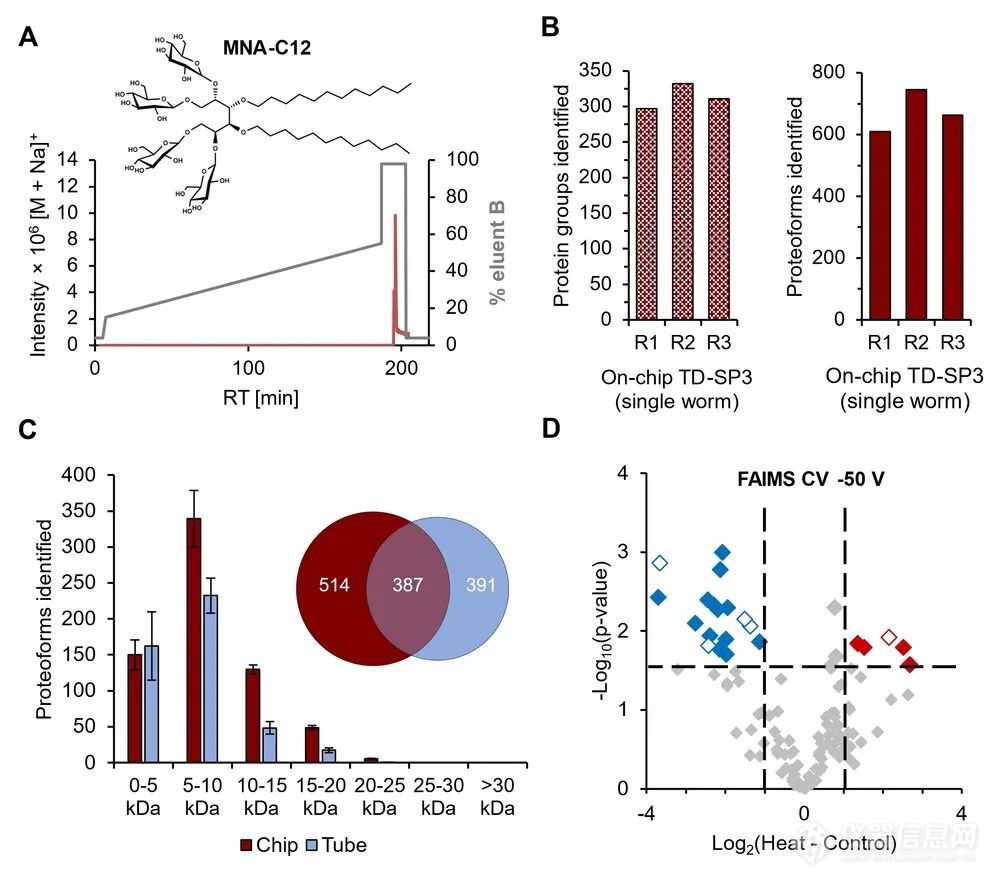
图3. 使用LC-MS 兼容洗涤剂和DMF-SP3分析单个秀丽隐杆线虫作者在此开发了一种易于使用的低上样量TD蛋白质组学样品制备工作流程,该方法将SP3与低成本的DMF液体处理系统相结合,可以量化单个模式生物少于1000个细胞的蛋白质丰度变化,具有高灵敏度,并且具有逐步优化的可能性。未来随着更大电极阵列的发展和可用性,DMF-SP3也将实现自动化、更高通量的TD纳米蛋白质组学,在Proteoform水平分析少数甚至单个哺乳动物细胞的细胞类型特异性蛋白质组组成差异。

