2022年8月,全球同意新药数量继续平稳。FDA同意8款新药(NDA/BLA),包括0款新获批的新分子实体药物(NDA:Type 1 - New Molecular Entity),2款生物制品药物(BLA),其间CIMERLI是全球首个FDA同意的可交换生物相似药;EMA新授权3款药品上市,其间2款新活性物质(NAS);NMPA同意3个品规(1个种类)立异药上市,属生物制品,为神州细胞的瑞帕妥单抗注射液。
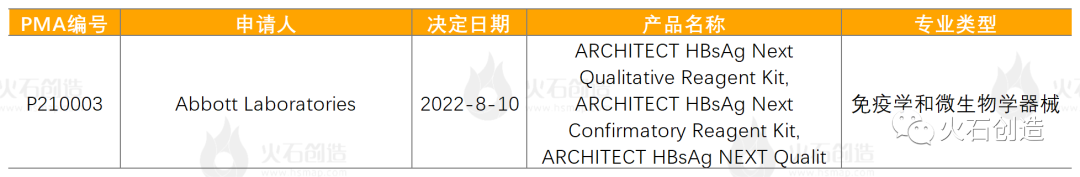
医疗器械方面,FDA有1个经过上市前同意(PMA)途径初次上市的产品。境内公示了10个三类医疗器械进入立异批阅绿色通道,同意了7个立异器械上市,境内医疗器械批阅会集在体外确诊试剂,共1034项,占33.31%。
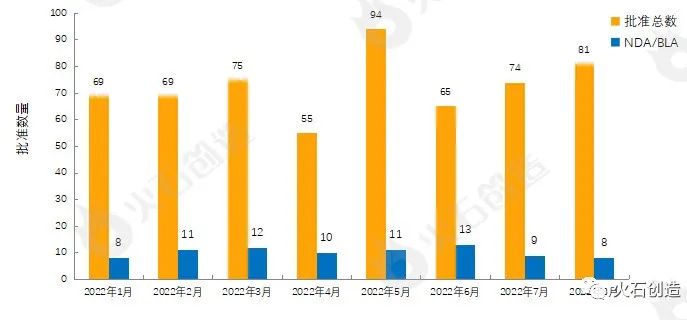
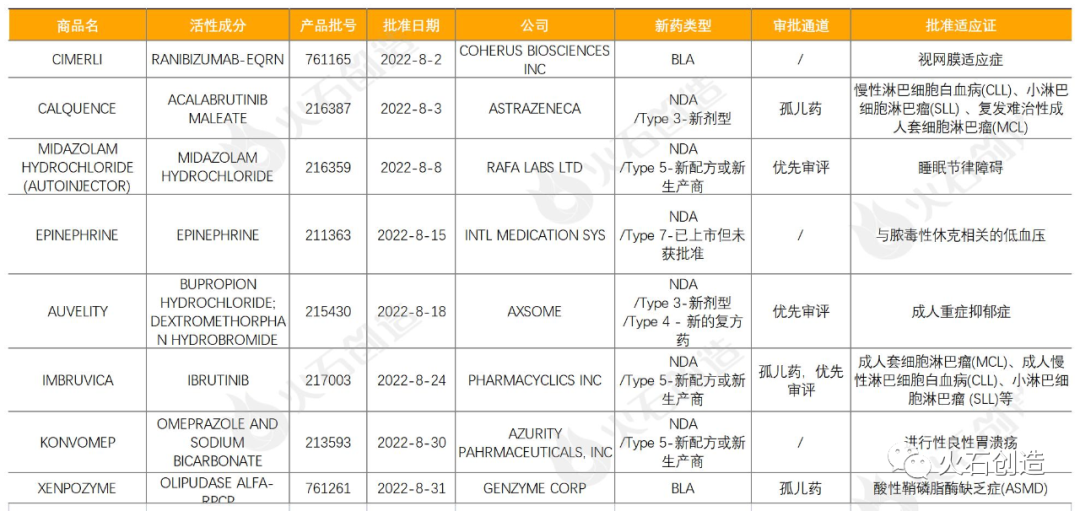
如图1,到2022年9月7日FDA官网发表,2022年8月FDA共完结81项药品初次同意(不包括暂时同意),其间NDA/BLA同意8款(不包括暂时同意),见表1。这中心还包括0款新获批的新分子实体药物(NDA:Type 1 - New Molecular Entity),2款生物制品药物(BLA)。
其间CIMERLI是全球首个FDA同意的可交换生物相似药,被同意可与诺华Lucentis(ranibizumab注射剂)交换,适用于Lucentis在美国获批的一切适应症;AUVELITY是首款获批用于抑郁症医治的口服NMDA(N-甲基D-天冬氨酸)受体拮抗剂,一起也是60年来抑郁症医治的里程碑式新打破,其为45mg右美沙芬与105mg安非他酮的缓释复方组合;赛诺菲旗下公司GENZYME CORP的立异酶替代疗法药物XENPOZYME是首个也是仅有一款获批专门用来医治酸性鞘磷脂酶缺乏症(ASMD)的药物,其于2022年3月和6月,别离获日本厚生劳作省、欧盟同意上市。
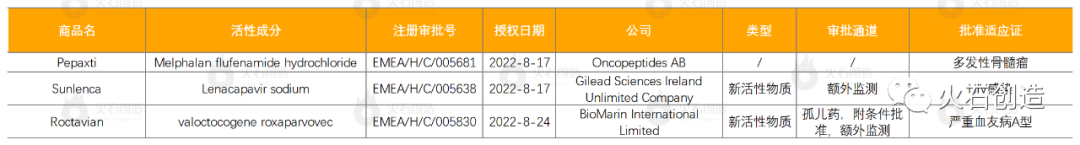
到2022年9月7日EMA官网发表,2022年1月至8月的引荐上市药品及新活性物质(NAS)数量状况见图2。2022年8月EMA未引荐药品上市。

其间吉祥德的Sunlenca(lenacapavir)是一款first-in-class的衣壳抑制剂,对其他现有药物没有已知的穿插耐药性,为现有抗病毒医治耐药的 HIV 感染者供给每六个月一次的长效新医治挑选;Roctavian是全球首款血友病腺相关病毒(AAV)基因疗法,此次欧盟附条件同意其上市,用来医治那些没有凝血因子Ⅷ抑制剂史且没有可检测到的AAV5型抗体的严峻血友病A型患者。
到2022年9月7日NMPA发表,2022年8月共同意国产初次注册药品60件。按剂型去重后,共42个药种类类(不同厂家出产同一药物按同一种类核算)。本月有3个品规(1个种类)1类立异药获批,属生物制品。2022年8月NMPA同意的1类立异药状况见表3。
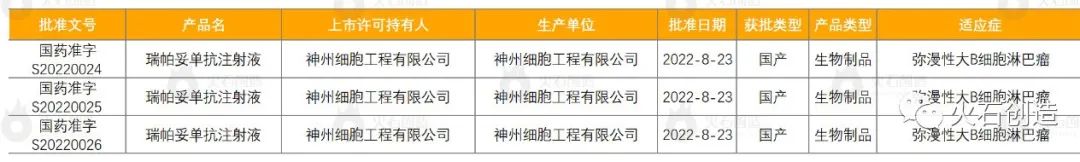
瑞帕妥单抗注射液是神州细胞自主研制的一种人鼠嵌合IgG1型抗CD20单克隆抗体,用来医治弥漫性大B细胞淋巴瘤(DLBCL)。DLBCL是最常见的非霍奇金淋巴瘤类型,是一种发展敏捷的侵袭性疾病,关于这类患者,抗CD20单抗是柱石医治药物。现在瑞帕妥单抗的获批将为更多患者供给一种新的医治挑选。
到2022年9月7日CDE官网发表,CDE共承办药品一致性点评受理号4176个,2022年8月共新增承办84个受理号。到2022年9月7日,共4626个品规上市药品经过一致性点评(包括视同经过1945个品规),本月共73个品规的药品经过一致性点评(包括视同经过13个品规),按剂型去重后,共45个药种类类。
现在一致性点评种类经过的注射剂共 1670个品规(254个种类),本月过评药品计47个品规(27个种类)的注射剂。2022年1月至8月经过一致性点评数量见图3。

到2022年9月7日,8月FDA共同意259个510(k)途径的产品,其间一类器械19个,二类器械236个,未分类4个。
经过对510(k)上市前告诉的器械依据美国医学专业用处进行分类,成果发现,8月产品获批类型最多的为骨科器械、一般医院和个人运用类器械、一般和整形手术器械、放射科器械与心血管器械,见图4。

图4 2022年8月经过FDA 510(k)途径获批上市产品类型散布状况
到2022年9月7日,2022年8月国家局公示了10个三类医疗器械进入立异批阅绿色通道,见表5。

到2022年9月7日,2022年8月国家局公示了7个三类立异器械获批上市,见表6。
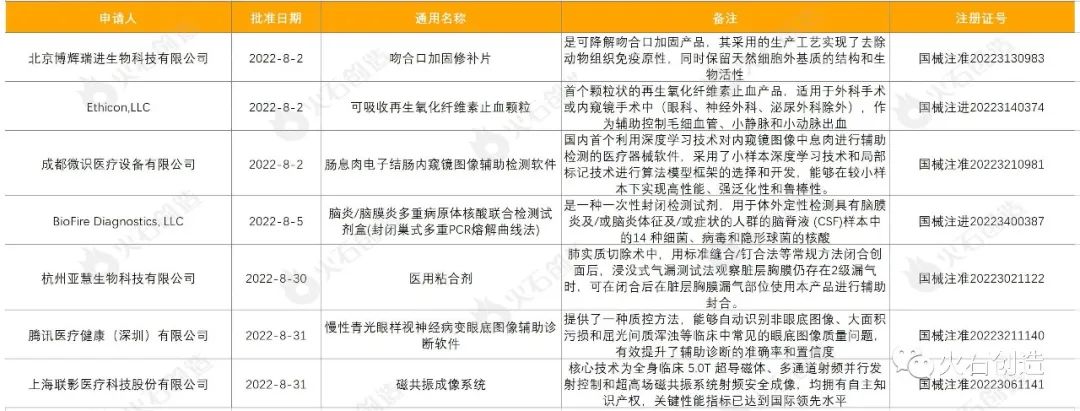
到2022年9月7日,2022年8月国家局共同意初次注册三类医疗器械产品191个,其间国产164个,进口27个。各省级药品监管部门8月共同意国产第二类医疗器械注册1261个,一类存案医疗器械1570个。
计算多个方面数据显现,体外确诊试剂数量最多,共1034项,占33.31%,基本上均为国产,为1019项。除体外确诊试剂,同意注册类别数量排前三位的别离为注输、护理和防护器械,临床查验器械和口腔科器械。

从地域散布上,2022年8月国产二、三类注册产品批件最多的依次为广东省(299件)、江苏省(219件)、湖南省(203件)三个区域,见图5。